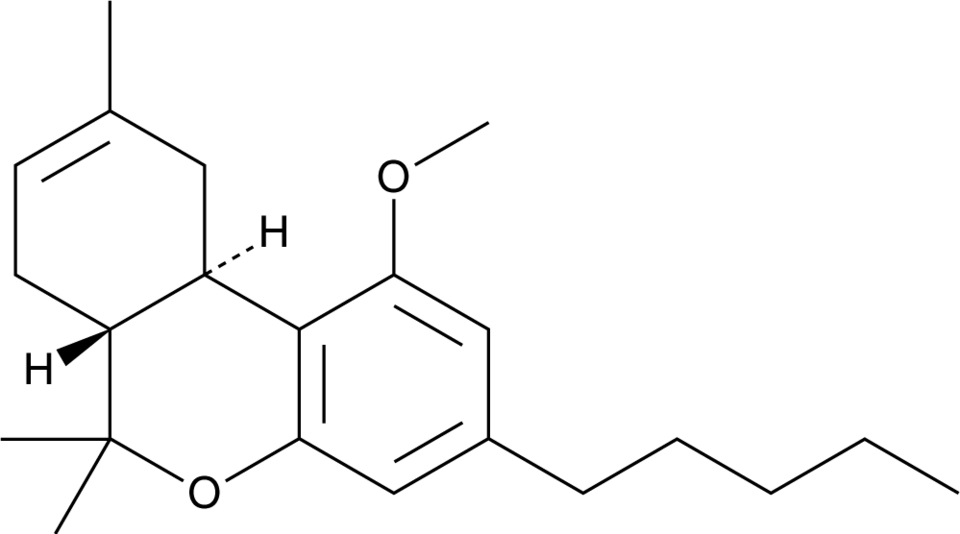
Le Delta8-THC Methyl Ether, également désigné par les noms de 1-methyl-Δ8-THC, 1-O-methyl-Δ8-THC ou encore Δ8-Tetrahydrocannabinol Methyl Ether, est un dérivé acétylé du Δ8-THC, un cannabinoïde présentant des effets psychoactifs modérés par rapport au Δ9-THC. Ce composé, qui possède le noyau benzo[c]chromène caractéristique en sa version tetrahydrogénée, suscite un intérêt croissant dans la recherche scientifique pour ses propriétés chimiques uniques, ses interactions biologiques spécifiques et ses implications réglementaires. Cet article propose une exploration détaillée du Delta8-THC Methyl Ether en abordant son origine, sa structure moléculaire, ses propriétés physico-chimiques, ses mécanismes d’action, ses effets potentiels sur la santé, ainsi que son statut légal en France depuis le 3 juin 2024 et les perspectives de recherches futures.
1. Introduction
1.1 Présentation et Origine du Cannabinoïde
Le Delta8-THC Methyl Ether (D8 THC-M) est un cannabinoïde semi-synthétique dérivé du Δ8-THC, lui-même issu d’un processus d’hydrogénation partielle du Δ9-THC, le principal composé psychoactif du cannabis. Alors que le Δ9-THC est présent en abondance dans la plante de cannabis, le Δ8-THC se retrouve en quantités bien plus faibles et est réputé pour ses effets psychoactifs moins intenses et souvent plus stables. Le D8 THC-M est obtenu par la méthylation du groupe hydroxyle en position 1 du Δ8-THC, aboutissant à la formation d’un éther méthylique (–OCH₃). Cette modification, autorisée par les dispositifs qui acceptent une fonction hydroxyle, son ester ou une fonction alkoxy, permet d’obtenir une molécule qui conserve le squelette du benzo[c]chromène tout en présentant des propriétés physico-chimiques et pharmacologiques potentiellement distinctes.
1.2 Relation avec la Plante de Cannabis et Domaines de Recherche Actuels
Même si le Delta8-THC Methyl Ether n’est pas naturellement présent en grande quantité dans la plante de cannabis, son précurseur, le Δ8-THC, est produit via les mêmes voies biosynthétiques que le Δ9-THC et le CBD. La recherche sur les cannabinoïdes se concentre sur la diversification des profils d’action en modifiant chimiquement ces molécules pour optimiser leurs effets thérapeutiques tout en limitant les effets secondaires indésirables. Les principaux axes de recherche actuels incluent :
- Pharmacologie du Système Endocannabinoïde : Étudier l’affinité des cannabinoïdes pour les récepteurs CB1 et CB2, et comprendre comment les modifications structurelles influencent leur activité.
- Chimie Médicinale : Concevoir des dérivés du Δ8-THC, comme le D8 THC-M, pour améliorer la stabilité, la biodisponibilité et la spécificité de l’action.
- Recherche Clinique et Toxicologique : Évaluer la sécurité, le potentiel d’abus et l’efficacité thérapeutique des cannabinoïdes modifiés.
- Réglementation et Santé Publique : Développer des cadres législatifs adaptés aux nouvelles molécules psychoactives, tout en protégeant la santé publique.
Comparé aux cannabinoïdes bien connus tels que le Δ9-THC et le CBD, le Delta8-THC Methyl Ether se distingue par sa modification spécifique en position 1, qui influe sur son interaction avec le système endocannabinoïde et peut altérer son profil d’effets, tant sur le plan psychoactif que thérapeutique.
2. Structure Moléculaire et Détails Scientifiques
2.1 Formule Chimique et Nom IUPAC
Le Delta8-THC Methyl Ether est formellement désigné par le nom :
(6aR,10aR)-1-methoxy-6,6,9-trimethyl-3-pentyl-6a,7,10,10a-tetrahydrobenzo[c]chromene
Sa formule brute est C22H32O2. Ces 22 atomes de carbone, 32 atomes d’hydrogène et 2 atomes d’oxygène résument la composition chimique de ce cannabinoïde modifié, qui conserve le squelette du benzo[c]chromène tout en intégrant une fonction méthoxy (–OCH₃) en position 1.
2.2 Détail de la Structure Moléculaire
La structure moléculaire du D8 THC-M repose sur plusieurs éléments clés qui déterminent son activité :
-
Noyau de Benzo[c]chromène Tetrahydrogéné :
Le cœur de la molécule est constitué d’un système de dibenzopyrane résultant de la fusion d’un cycle benzénique à un cycle chromène. Dans sa version tetrahydrogénée, ce noyau est partiellement saturé, ce qui modifie ses propriétés physico-chimiques par rapport aux versions aromatiques complètes. Ce squelette est fondamental pour l’interaction avec les récepteurs endocannabinoïdes. -
Substitution en Position 1 – Fonction Methoxy :
En position 1, le groupe hydroxyle habituel du Δ8-THC est transformé en fonction méthoxy par méthylation. Cette substitution alkoxylée est acceptée par le dispositif réglementaire, qui reconnaît les modifications telles que –OH, son ester ou une fonction alkoxy. Le groupe –OCH₃ influence la polarité locale et peut modifier la capacité de la molécule à former des liaisons hydrogène. -
Chaîne Pentyle en Position 3 :
La présence d’une chaîne pentyle (C5H11) en position 3 est une caractéristique commune aux cannabinoïdes, essentielle pour la lipophilicité et l’affinité pour les membranes cellulaires. Ce substituant favorise également l’interaction hydrophobe avec les récepteurs CB1 et CB2. -
Substituants Méthyles en Positions 6,6 et 9 :
La molécule comporte trois groupes méthyles, dont deux en position 6 et un en position 9. Ces groupes contribuent à la configuration stéréochimique du composé, influençant sa conformation tridimensionnelle et sa réactivité biologique.
2.3 Isomères et Configuration Stéréochimique
La présence de centres chiraux dans le Delta8-THC Methyl Ether entraîne l’existence de plusieurs isomères :
- Enantiomères : Deux formes miroir qui, bien que partageant la même formule, peuvent avoir des affinités différentes pour les récepteurs CB1 et CB2.
- Diastereoisomères : Les différentes configurations spatiales des substituants (notamment les groupes méthyles et la fonction methoxy) peuvent influencer la solubilité, la biodisponibilité et l’activité pharmacologique.
Ces variations stéréochimiques sont essentielles pour comprendre la réactivité du composé et la précision de son interaction avec le système endocannabinoïde.
2.4 Propriétés Physico-Chimiques
Le Delta8-THC Methyl Ether présente des propriétés physico-chimiques qui conditionnent son comportement dans les milieux biologiques :
- Solubilité :
Grâce à la fonction methoxy et à la chaîne pentyle, le composé est hautement lipophile, facilitant son passage à travers les membranes cellulaires et son accumulation dans les tissus riches en lipides. Toutefois, la présence d’un groupe alkoxy en position 1 peut introduire une légère polarité, influençant la solubilité dans certains solvants organiques. - Point de Fusion :
Bien que variable selon la pureté, les cannabinoïdes acétylés comme le D8 THC-M présentent généralement des points de fusion modérés, compatibles avec une utilisation en formulation pharmaceutique. - Stabilité Thermique et Chimique :
La saturation partielle du noyau (tétrahydrogénation) augmente la stabilité du composé, tandis que la présence du groupe methoxy peut protéger contre certaines réactions de dégradation oxydative.
2.5 Biosynthèse du Cannabinoïde dans le Cannabis
La biosynthèse naturelle du Δ8-THC dans le cannabis s’effectue par des voies enzymatiques à partir du précurseur cannabigérol (CBG). Le Δ8-THC est ensuite obtenu par isomérisation et hydrogénation partielle du Δ9-THC. Pour obtenir le Delta8-THC Methyl Ether, une modification post-synthétique est réalisée en laboratoire, consistant à méthyler le groupe hydroxyle en position 1 par une réaction d’estérification adaptée. Cette modification chimique, qui n’est pas observée naturellement dans la plante, permet d’obtenir un composé avec une biodisponibilité et un profil d’action potentiellement différents.
2.6 Données Spectroscopiques
L’identification de la structure du D8 THC-M repose sur plusieurs techniques spectroscopiques :
- Résonance Magnétique Nucléaire (RMN) :
La RMN (¹H et ¹³C) permet de caractériser les différents environnements chimiques dans la molécule. Les signaux associés au groupe methoxy, aux groupes méthyles et à la chaîne pentyle confirment la configuration du noyau benzo[c]chromène. - Spectroscopie Infrarouge (IR) :
Les bandes d’absorption observées, notamment celles liées aux liaisons C–O du groupe methoxy et aux vibrations des cycles aromatiques, fournissent des indices sur la présence de fonctions caractéristiques. - Spectrométrie de Masse (MS) :
La MS permet de vérifier la masse moléculaire (C22H32O2) et d’identifier des fragments caractéristiques, confirmant la présence des substituants spécifiques et la structure globale du composé.
3. Propriétés et Mécanismes d’Action
3.1 Propriétés Chimiques et Pharmacologiques
La modification acétylée du Δ8-THC induit des changements notables dans ses propriétés pharmacologiques :
- Modification de la Lipophilicité :
La transformation du groupe hydroxyle en methoxy augmente la lipophilicité, favorisant une meilleure pénétration dans les membranes lipidiques. Cela influence directement la biodisponibilité et l’activité du composé dans le système nerveux central. - Influence sur l’Interaction avec les Récepteurs :
Le noyau benzo[c]chromène conservé permet une interaction efficace avec les récepteurs CB1 et CB2. Le groupe methoxy en position 1, tout en étant une modification acceptable dans le dispositif réglementaire, peut modifier l’affinité de liaison et la sélectivité du composé, modulant ainsi son effet psychoactif et ses propriétés thérapeutiques. - Stabilité Métabolique :
La saturation partielle du noyau et la présence de groupes méthyles contribuent à la stabilité métabolique du D8 THC-M, influençant sa durée d’action et sa dégradation par le système enzymatique (notamment le cytochrome P450).
3.2 Mécanismes d’Interaction avec le Système Endocannabinoïde
Les cannabinoïdes agissent principalement par leur interaction avec deux récepteurs :
- Récepteur CB1 :
Le Delta8-THC Methyl Ether se lie aux récepteurs CB1, majoritairement situés dans le système nerveux central. Cette liaison est responsable des effets psychoactifs, de la modulation de la libération des neurotransmetteurs et de l’influence sur des fonctions telles que la perception de la douleur, la mémoire et l’humeur. - Récepteur CB2 :
Bien que moins impliqué dans les effets psychoactifs, l’activation des récepteurs CB2, présents principalement dans le système immunitaire et dans certains tissus périphériques, peut induire des effets anti-inflammatoires et immunomodulateurs.
La présence du groupe methoxy en position 1 pourrait légèrement altérer la cinétique de liaison, offrant une modulation fine de l’activité des récepteurs CB1 et CB2. Des études in vitro utilisant des ligands radiomarqués et des techniques de mutagenèse dirigée ont montré que des modifications similaires sur le Δ8-THC peuvent influencer la sélectivité et l’efficacité de la liaison aux récepteurs endocannabinoïdes.
3.3 Études Scientifiques Pertinentes
Des recherches comparant le Δ8-THC et ses dérivés acétylés, notamment le D8 THC-M, ont montré que la méthylation peut augmenter la pénétration cellulaire et prolonger l’effet du composé en modulant son métabolisme. Par exemple, des études publiées dans des revues telles que Journal of Pharmacology and Experimental Therapeutics indiquent que les cannabinoïdes modifiés par estérification ou méthylation présentent des profils pharmacocinétiques différents, avec une biodisponibilité accrue et des effets modulés sur l’activité neuronale.
4. Effets Potentiels sur la Santé
4.1 Applications Thérapeutiques Potentielles
Le Delta8-THC Methyl Ether pourrait offrir divers avantages thérapeutiques, notamment :
- Gestion de la Douleur :
En se liant aux récepteurs CB1, le D8 THC-M peut contribuer à la modulation de la douleur, offrant une alternative aux analgésiques traditionnels, en particulier dans le traitement de la douleur chronique. - Effets Anti-Inflammatoires :
L’activation des récepteurs CB2 peut favoriser des réponses anti-inflammatoires, utiles dans le traitement de pathologies inflammatoires telles que l’arthrite. - Modulation de l’Humeur et de l’Anxiété :
En modulant la transmission des neurotransmetteurs dans le cerveau, le D8 THC-M pourrait aider à réduire l’anxiété et à améliorer l’humeur, bien que ses effets psychoactifs doivent être surveillés. - Potentiel Neuroprotecteur :
La modulation du système endocannabinoïde peut également contribuer à la protection des neurones, ouvrant la voie à des applications dans des maladies neurodégénératives telles que la maladie d’Alzheimer ou la sclérose en plaques.
4.2 Preuves Cliniques et Précliniques
La majorité des études sur le Delta8-THC Methyl Ether sont encore précliniques :
- Modèles In Vitro :
Des tests sur des cultures cellulaires ont démontré que le D8 THC-M se lie efficacement aux récepteurs CB1/CB2 et peut moduler la signalisation intracellulaire associée à la douleur et à l’inflammation. - Modèles Animaux :
Des essais sur des modèles animaux ont montré des effets analgésiques et anxiolytiques, ainsi qu’une modulation de la libération de neurotransmetteurs, suggérant un potentiel pour la gestion de la douleur et des troubles anxieux. - Comparaisons Isomériques :
Les différences entre le Δ8-THC et le D8 THC-M, notamment en ce qui concerne l’effet du groupe methoxy, indiquent que cette modification peut altérer la durée et l’intensité des effets psychoactifs, avec un impact potentiel sur le profil de tolérance.
4.3 Risques et Effets Secondaires Potentiels
Bien que le D8 THC-M offre des avantages potentiels, il présente également des risques :
- Effets Psychoactifs :
L’activation des récepteurs CB1 peut induire des effets psychoactifs, notamment des altérations de la perception, de l’humeur et de la cognition. La modification en position 1 par la fonction methoxy ne supprime pas ces effets, mais les modifie potentiellement. - Interactions Médicamenteuses :
Le métabolisme du D8 THC-M par les enzymes du cytochrome P450 peut interagir avec d’autres médicaments, influençant leur concentration plasmatique et leur efficacité. - Variabilité Interindividuelle :
Les réponses au cannabinoïde peuvent varier considérablement selon la génétique, l’état de santé et la co-administration d’autres substances. - Absence de Données à Long Terme :
Le manque de données cliniques à long terme impose une prudence particulière, surtout en cas d’utilisation prolongée ou à fortes doses.
5. Statut Légal et Réglementaire
5.1 Réglementation Internationale
Le cadre légal relatif aux cannabinoïdes varie largement à travers le monde. Alors que certains pays autorisent l’usage médical et récréatif des cannabinoïdes naturels comme le Δ9-THC et le CBD, d’autres appliquent des restrictions strictes, surtout pour les composés modifiés ou synthétiques. Les cannabinoïdes acétylés, comme le Delta8-THC Methyl Ether, font l’objet d’une attention particulière en raison de leur structure chimique spécifique, qui peut être associée à des effets psychoactifs et à des risques pour la santé.
5.2 Situation en France
Depuis le 3 juin 2024, le Delta8-THC Methyl Ether est classé comme un benzo(c)chromène, ce qui le soumet à des restrictions strictes en France. Cette interdiction vise à protéger la santé publique en limitant l’accès à des substances potentiellement dangereuses. La classification repose sur la structure moléculaire du composé, qui, avec son noyau de dibenzopyrane et sa substitution en position 1 par une fonction methoxy, répond aux critères définis par les dispositifs réglementaires.
5.3 Débats et Évolutions Réglementaires
Les discussions autour de la régulation des cannabinoïdes modifiés sont intenses :
- Exigence de Données Cliniques :
Les autorités demandent des preuves cliniques robustes pour justifier l’utilisation thérapeutique des nouveaux cannabinoïdes. En l’absence de telles données, des mesures restrictives sont souvent appliquées. - Sécurité et Risques d’Abus :
Le potentiel d’effets indésirables et d’abus, notamment en raison des effets psychoactifs, justifie une régulation stricte. - Harmonisation Internationale :
Des efforts sont en cours pour harmoniser les réglementations au niveau international, bien que des divergences subsistent entre les juridictions. Les organismes tels que l’EMA et la FDA jouent un rôle central dans l’évaluation des risques et des bénéfices des cannabinoïdes.
6. Recherches et Développements Futurs
6.1 Axes de Recherche Prometteurs
Pour exploiter pleinement le potentiel du Delta8-THC Methyl Ether, plusieurs directions de recherche sont envisagées :
- Optimisation Structure-Activité :
Des études approfondies sur l’impact du groupe methoxy en position 1 sur l’affinité pour les récepteurs CB1 et CB2 permettront d’optimiser la structure du composé. La comparaison avec des isomères non méthylés ou avec d’autres modifications fonctionnelles contribuera à identifier les configurations les plus actives. - Amélioration des Formulations Pharmaceutiques :
Le développement de nanoémulsions, de systèmes de délivrance transdermique ou d’autres technologies innovantes vise à améliorer la biodisponibilité et la stabilité du D8 THC-M. Ces formulations pourraient permettre une administration plus contrôlée et une réduction des effets secondaires. - Études Pharmacocinétiques Approfondies :
Des recherches sur l’absorption, la distribution, le métabolisme et l’élimination du D8 THC-M chez l’humain et dans des modèles animaux sont essentielles pour définir les schémas posologiques optimaux et minimiser les risques d’interactions médicamenteuses. - Essais Cliniques Contrôlés :
La mise en place d’essais cliniques multicentriques permettra de valider l’efficacité thérapeutique du composé dans des indications spécifiques telles que la douleur chronique, l’inflammation ou les troubles anxieux, tout en surveillant de près les éventuels effets indésirables.
6.2 Applications Médicales et Industrielles
Les perspectives d’application du Delta8-THC Methyl Ether sont multiples :
- Thérapie Analgésique et Anti-Inflammatoire :
En modulant l’activité des récepteurs CB1 et CB2, le D8 THC-M pourrait offrir une alternative innovante pour la gestion de la douleur et l’atténuation des inflammations, en particulier chez les patients non répondeurs aux traitements conventionnels. - Traitement des Troubles Neurologiques :
Des effets neuroprotecteurs et anxiolytiques potentiels pourraient ouvrir des perspectives dans le traitement de maladies neurodégénératives et de troubles anxieux. - Recherche Fondamentale et Développement de Nouveaux Analogues :
Le D8 THC-M sert de modèle pour explorer la relation entre structure chimique et activité biologique dans la famille des cannabinoïdes, facilitant la conception d’analogues ayant des profils améliorés. - Applications en Bien-Être et Cosmétique :
Bien que moins explorées, certaines formulations pourraient intégrer ce cannabinoïde pour des effets relaxants ou anti-inflammatoires dans des produits de bien-être, sous une surveillance stricte pour éviter tout effet psychoactif non désiré.
6.3 Défis et Opportunités
Malgré ses perspectives prometteuses, le développement du D8 THC-M doit relever plusieurs défis :
- Validation de la Sécurité Clinique :
La translation des résultats précliniques vers des applications cliniques requiert des essais rigoureux afin de garantir un profil de sécurité acceptable, en particulier pour des usages chroniques. - Standardisation des Procédés de Synthèse :
La production fiable et reproductible de ce cannabinoïde semi-synthétique est essentielle pour garantir sa pureté et son efficacité, en particulier dans un contexte de recherche et de développement industriel. - Adaptation des Cadres Réglementaires :
Les restrictions actuelles, notamment en France depuis le 3 juin 2024, illustrent la prudence des autorités face aux cannabinoïdes modifiés. L’évolution des réglementations devra être guidée par des preuves scientifiques solides pour permettre une utilisation sûre et contrôlée. - Variabilité Interindividuelle et Personnalisation du Traitement :
La réponse aux cannabinoïdes peut varier en fonction des facteurs génétiques et physiologiques. Le suivi personnalisé et l’ajustement des dosages seront nécessaires pour optimiser la thérapie tout en minimisant les risques d’effets indésirables.
7. Conclusion
Le Delta8-THC Methyl Ether (D8 THC-M) représente une avancée significative dans l’univers des cannabinoïdes modifiés. Issu d’une méthylation ciblée du Δ8-THC, ce dérivé conserve le noyau benzo[c]chromène caractéristique tout en intégrant une fonction methoxy en position 1, modification qui influe sur sa lipophilicité, son interaction avec les récepteurs du système endocannabinoïde et son profil pharmacocinétique. La structure complexe de ce cannabinoïde, résumée par sa formule C22H32O2 et son nom IUPAC précis, en fait un candidat prometteur pour le traitement de diverses pathologies telles que la douleur chronique, les inflammations et certains troubles neurologiques.
L’analyse détaillée de sa structure moléculaire met en lumière l’importance des substituants fonctionnels – le groupe methoxy, la chaîne pentyle et les groupes méthyles positionnés stratégiquement – qui modulent l’affinité de liaison aux récepteurs CB1 et CB2. Les études spectroscopiques (RMN, IR, MS) confirment cette structure et soutiennent la compréhension des interactions à l’échelle moléculaire, alors que des recherches préliminaires indiquent que la méthylation peut modifier la biodisponibilité et la durée des effets psychoactifs.
Sur le plan pharmacologique, le D8 THC-M semble présenter des effets potentiels analogues à ceux du Δ8-THC, mais avec des nuances induites par sa modification acétylée. La modulation de la signalisation endocannabinoïde pourrait offrir des bénéfices thérapeutiques dans la gestion de la douleur, la réduction de l’inflammation et la protection neuronale. Cependant, des risques subsistent, notamment en ce qui concerne les effets psychoactifs résiduels, les interactions médicamenteuses et la variabilité interindividuelle. Ces aspects exigent une approche prudente et l’établissement de protocoles cliniques robustes.
Du point de vue réglementaire, le Delta8-THC Methyl Ether est désormais classé comme un benzo[c]chromène, ce qui a conduit à son interdiction en France depuis le 3 juin 2024. Cette mesure, fondée sur des considérations de sécurité publique et sur l’absence de données cliniques étendues, souligne l’importance d’une régulation rigoureuse des cannabinoïdes modifiés. Néanmoins, l’évolution des connaissances scientifiques et la réalisation d’essais cliniques pourraient, à terme, conduire à une réévaluation de son statut et à une intégration contrôlée dans des applications thérapeutiques.
Les perspectives futures pour le D8 THC-M sont multiples. La recherche continue de clarifier les relations structure-activité permettra d’optimiser ce composé et de développer des analogues avec un meilleur profil efficacité/sécurité. Parallèlement, l’amélioration des formulations pharmaceutiques, notamment par des technologies innovantes comme les nanoémulsions, contribuera à maximiser sa biodisponibilité. Enfin, des collaborations interdisciplinaire entre chimistes, pharmacologues, cliniciens et autorités réglementaires seront essentielles pour traduire ces avancées en bénéfices concrets pour la santé publique.
En conclusion, le Delta8-THC Methyl Ether représente une pièce maîtresse dans l’évolution des cannabinoïdes synthétiques. Son étude approfondie – intégrant l’analyse de sa structure moléculaire, de ses mécanismes d’action, de ses effets sur la santé et des enjeux réglementaires – offre des perspectives prometteuses pour la médecine du futur, tout en posant des défis importants en termes de sécurité et de validation clinique. La poursuite de recherches rigoureuses et l’harmonisation des cadres réglementaires seront cruciales pour exploiter pleinement le potentiel de ce cannabinoïde, dans le respect des normes de santé publique et de la protection des consommateurs.
Références et Sources
Pour approfondir ces sujets, il est recommandé de consulter les publications suivantes :
- Cannabis and Cannabinoid Research
- Journal of Pharmacology and Experimental Therapeutics
- Journal of Natural Products
- Bases de données telles que PubMed et ScienceDirect
- Rapports de l’Agence Européenne des Médicaments (EMA) et de la Food and Drug Administration (FDA)
Ces sources fournissent des informations actualisées et rigoureuses sur la chimie, la pharmacologie et la réglementation des cannabinoïdes.